复旦/上海理工团队: 3D打印支撑结构,GelMA/PLMA制备囊膜混浊模型
时间:2024-09-13 14:40 来源: EFL生物3D打印与生物制造 作者:admin 点击:次
| 后发性白内障(PCO),又称后囊膜混浊,是白内障术后一种主要的远期并发症,,术后1-5年的发病率在成人中为20%-40%,在儿童中则高达100%。近年来,虽然有多种措施尝试减少PCO的发生,但目前PCO发生发展机制尚未完全清楚,因此进一步完善和发展PCO的预防和治疗策略,对PCO发生机制进行深入研究至关重要。 近期,复旦大学附属医院竺向佳教授、罗怡教授以及上海理工大学戴博教授团队在《Regenerative Biomaterials》上发表了题为“Fabrication of a 3D bioprinting model for posterior capsule opacification using GelMA and PLMA hydrogel-coated resin”的研究论文,提出了一种新的PCO模型用于模拟白内障手术后透镜囊的解剖结构。研究人员利用EFL品牌的投影式光固化生物3D打印机(EFL-BP8601 Pro)并结合了光敏树脂制备了一个刚性中空底座和盖子的外部支撑结构,后将水凝胶旋涂在树脂支架上,构建出透镜囊结构。后期通过一系列染色技术评估了各种水凝胶组合物的生物相容性和对细胞功能的影响,并探究了多种具有抗炎和抗增殖特性的药物对人透镜上皮细胞(HLEC)的作用,表明了PCO模型为研究PCO的发病机制和探索潜在的治疗干预措施提供了一个有价值的实验平台。 
为探索PCO的病理机制和药物干预策略,研究工作者们开发了多种体内和体外模型,但这些模型在三维动态培养、仿生袋状支撑、微环境的模拟和干预等关键领域仍存在局限性。而本研究探讨了一种新的体外PCO模型的构建方法,先基于白内障手术后透镜的解剖结构和透镜囊的结构设计出三维模型,采用基于光敏树脂的生物3D打印工艺构建出稳定的外层结构以提供有效的支撑,后为了更好的模拟囊袋的囊壁结构,将水凝胶薄涂在支架表面以建立良好的生长微环境。整体PCO模型采用开合式设计,便于模型精确定位、实验干预和染色观察。 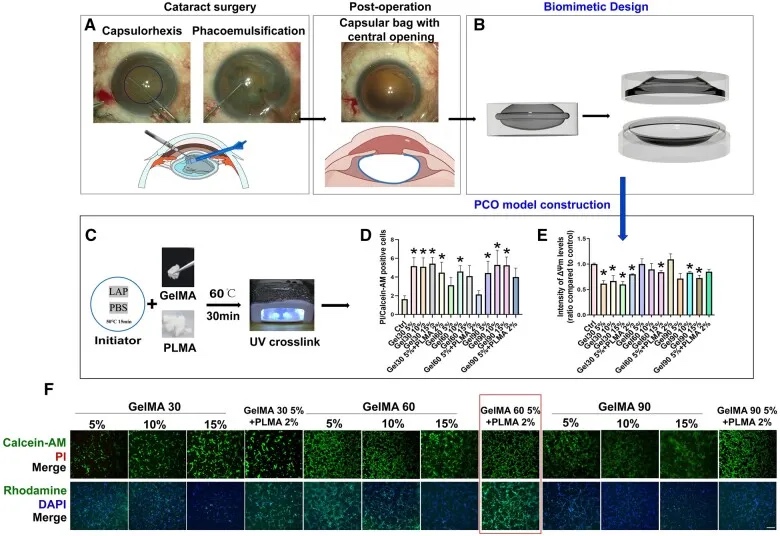
图1 PCO模型的设计和构建
为确定最佳水凝胶混合物作为PCO模型的超薄涂层,研究人员通过评估不同浓度以及材料条件下细胞的可渗透性和生物相容性,选择了5wt% GelMA60和2wt% ε-PLMA作为最佳混合物。而后为了更好的复制透镜囊的晶状体结构并为人晶状体上皮细胞(HLEC)培养创造最佳条件,比较了用水凝胶涂覆PCO模型的各种方法,发现采用旋涂法且转速2000 rpm时得到的水凝胶涂层具有优异的生物相容性、稳定性、抗菌活性和低氧化应激发生率,为HLEC提供了有利生长环境。 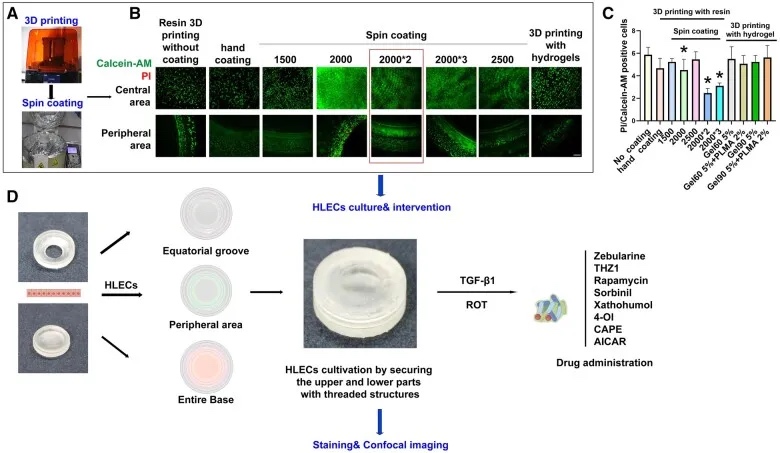
图2 PCO模型构建、干预和分析示意图
研究人员对比了培养皿培养、水凝胶3D打印培养、PCO模型构建三种方法下细胞的活性以及脂质过氧化水平,验证了用于PCO模型表面的水凝胶涂层的旋涂技术为HLEC培养提供了最佳环境,表明了所提出的PCO模型构建方式确保了机械支撑、形态稳定性和生物相容性特征之间的平衡。 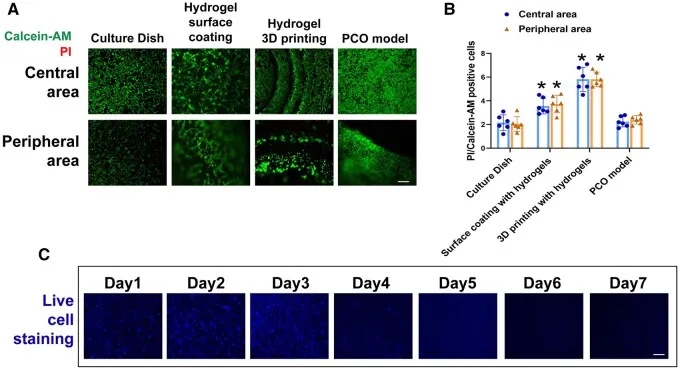
图3 PCO模型生物材料相容性评价
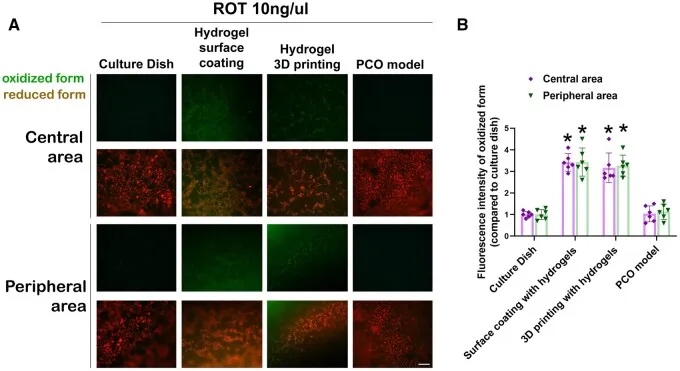
图4 PCO模型氧化应激水平的评价
研究人员基于PCO模型探究了所选择的8种药物的抗细胞凋亡、抗氧化应激和抗炎特性,通过评估药物对HLEC的作用证实了AICAR、雷帕霉素、4-OI在PCO模型中显著抑制HLEC的增殖和迁移,表明了AICAR、雷帕霉素、4-OI是药物开发的理想靶点。 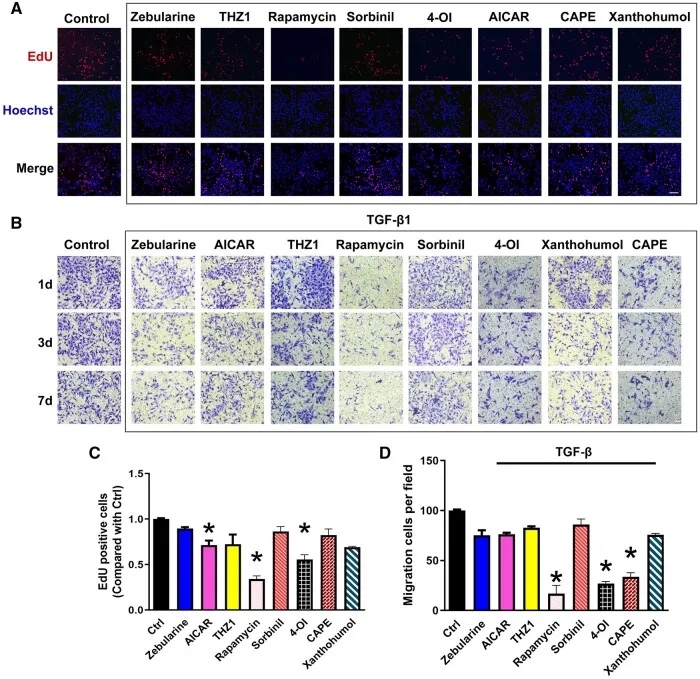
图5 PCO模型中药物治疗后的细胞迁移
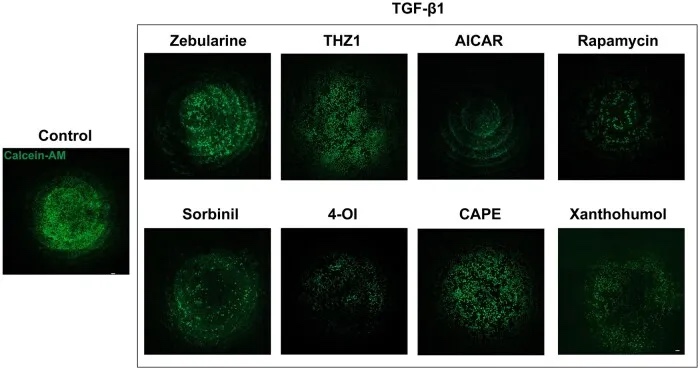
图6 药物治疗后PCO模型中的细胞迁移评价
综上所述,本文成功开发了一种新的PCO模型,该模型精心设计的参数模拟了白内障手术后透镜囊的状态,而3D打印的中空底座提供了稳定性和支撑,并应用GelMA和PLMA复合水凝胶的微生物涂层为HLEC生长创造了最佳的微环境。该模型不仅可用于研究PCO的发病机制,还可用于各种药物干预研究,分析不同药物干预PCO发生发展的效果,为精确干预提供实验依据。 文章来源: https://doi.org/10.1093/rb/rbae020 (责任编辑:admin) |