心肌梗死(MI)修复面临的关键挑战在于成年心肌细胞再生能力有限,且传统治疗(如血管成形术)仅聚焦局部血运重建,忽视神经调控对心脏生理活动的系统性作用。现有神经调节策略(如迷走神经刺激、药物激活)因信号控制复杂和潜在副作用,临床应用受限。此外,神经干细胞(NSCs)虽具分化为神经元的潜力,但其分化方向难控,依赖生长因子的传统诱导方法存在稳定性和生物安全性问题。
针对上述痛点,中国科学院上海硅酸盐研究所吴成铁研究员团队开发了基于3D生物打印技术的“预神经化”支架。该团队将硅酸锶(SrSiO₃)微粒子与NSCs结合,利用3D打印构建多孔支架,通过Sr²⁺和Si²⁻离子释放诱导NSCs定向分化为成熟神经元,形成具有神经调节功能的活性支架。体内外实验表明,该支架可增强心肌细胞成熟和同步收缩,激活昼夜节律相关基因(如Per2、Usp24)促进心肌修复,改善心梗大鼠心脏功能。相关工作以“Inorganic Biomaterials Inducing Scaffolds Pre㎞euralization for Infarcted Myocardium”为题发表在《Advanced Materials》上。论文第一作者为上海硅酸盐所博士研究生王之栩,通讯作者为吴成铁研究员。
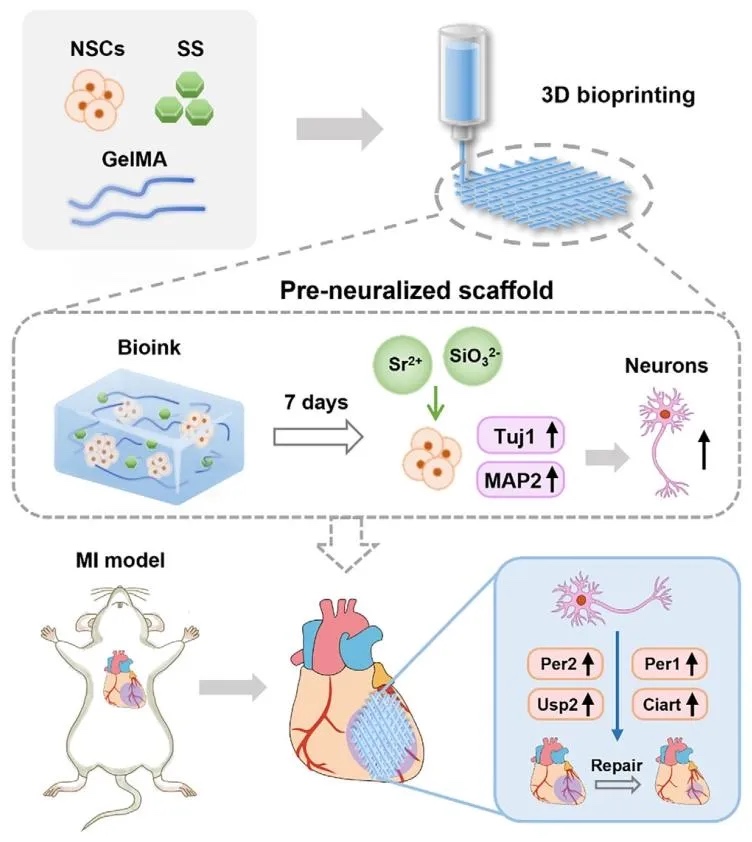
预神经化支架的设计制备及其用于梗死心肌修复的示意图。由于硅酸锶的作用,3D 生物打印支架中的神经干细胞被诱导分化为成熟神经元。将预神经化支架植入心肌梗死大鼠体内后,其通过调控昼夜节律相关基因,加速了梗死心肌的修复。
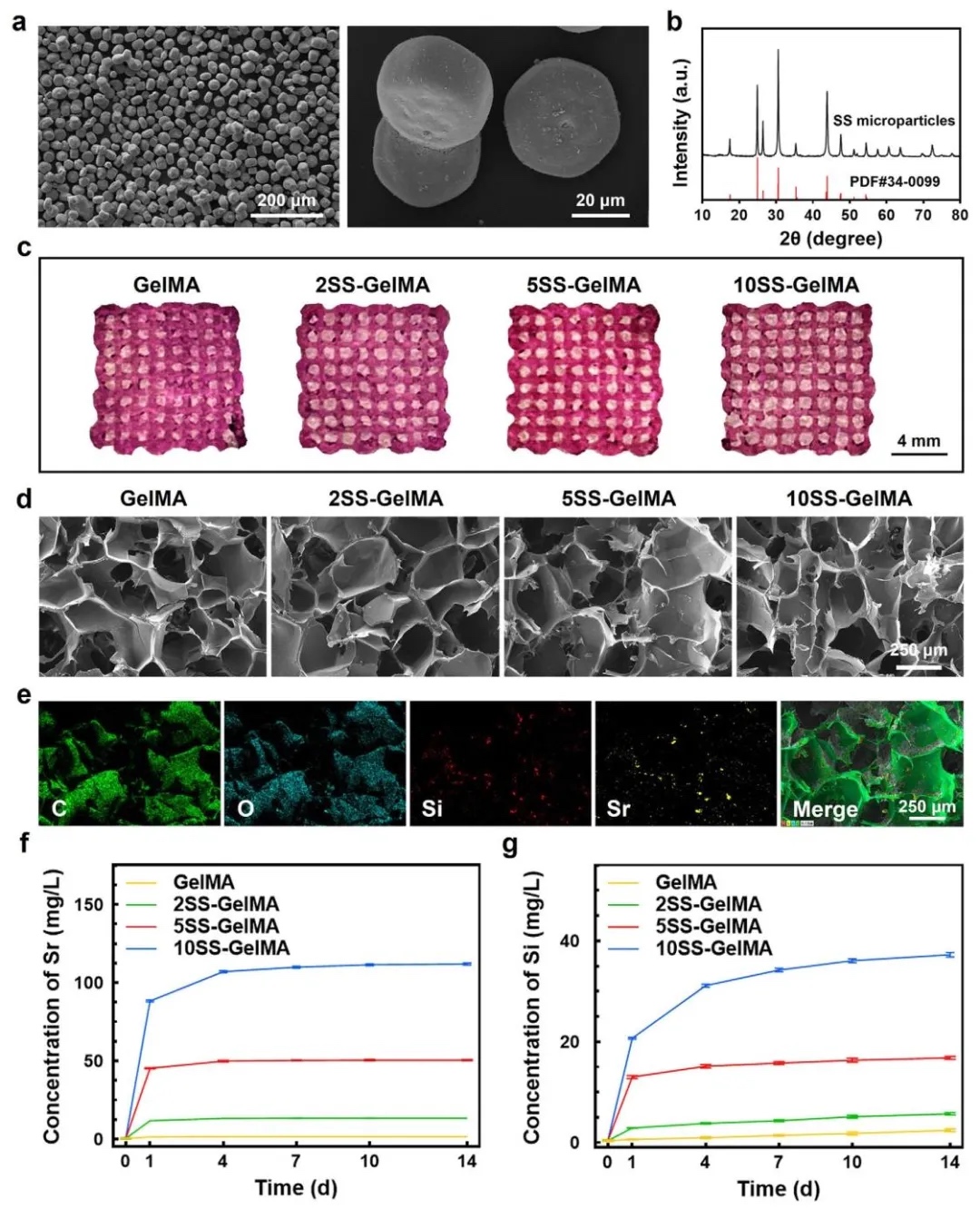
1. 硅酸锶微粒子及3D打印支架的表征,通过扫描电子显微镜(SEM)、X射线衍射(XRD)、流变学分析和离子释放实验等方法,研究了不同浓度硅酸锶(SS)微粒子(0%、2%、5%、10%)的形貌、物相、生物墨水打印性能及Sr/Si离子释放规律。结果表明,SS微粒子呈六方棱柱形,5SS-GelMA支架兼具良好打印性和离子释放稳定性,Sr/Si离子在7天内基本完全释放,与神经干细胞(NSCs)分化时间窗匹配。
图1. 硅酸锶微粒子及3D打印支架的表征。
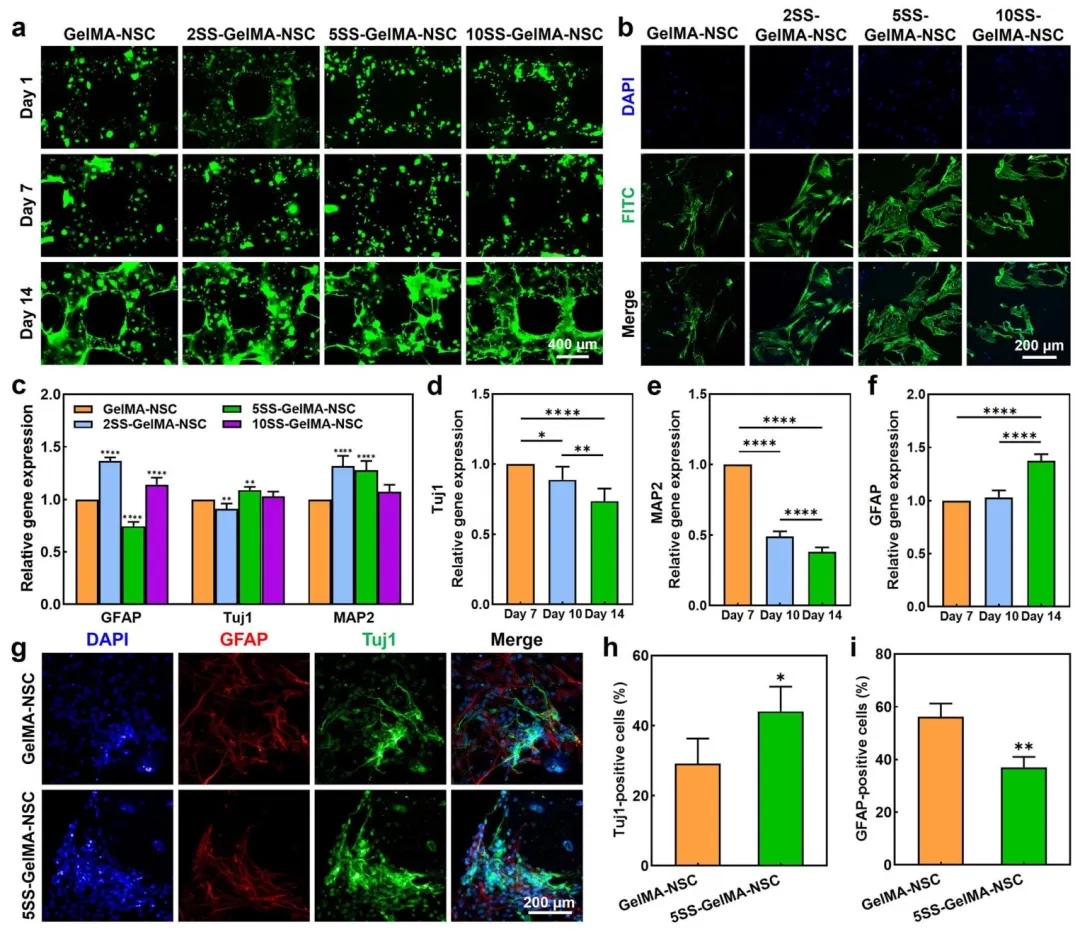
2. 预神经化支架的体外神经分化行为,利用实时定量PCR(RT-qPCR)、免疫荧光染色和EdU增殖实验,研究了NSCs在不同SS浓度支架中的分化、增殖及毒性反应。结果显示,5% SS浓度(5SS-GelMA-NSC)显著促进NSCs向神经元分化(Tuj1+和MAP2+细胞比例升高),抑制星形胶质细胞标记物GFAP表达,且7天为最佳预神经化时间,此时离子释放与分化效果同步。
图2. 硅酸锶微粒子诱导3D打印神经干细胞负载支架的神经元分化行为。
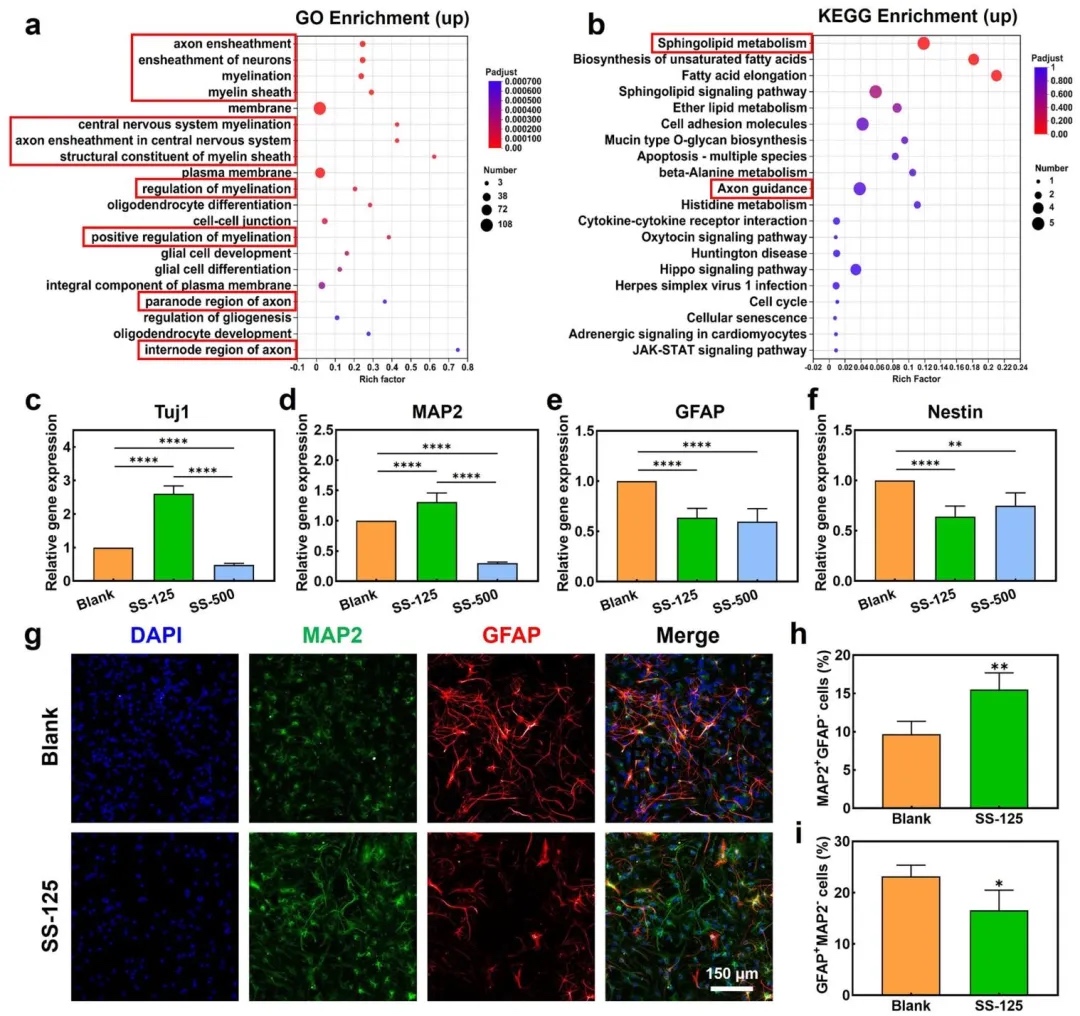
3. 硅酸锶促进NSCs分化的机制,通过转录组测序、离子浓度梯度实验和免疫荧光染色,分析了SS调控NSCs分化的分子通路及离子作用机制。结果表明,SS通过激活轴突导向和鞘脂代谢相关基因(如MAP2),且Sr/Si离子浓度为125 μg/mL时可有效诱导神经元成熟,过高浓度(500 μg/mL)则具细胞毒性。
图3. 硅酸锶促进神经干细胞向神经元分化的机制及不同浓度提取液中NSCs的分化行为表征。
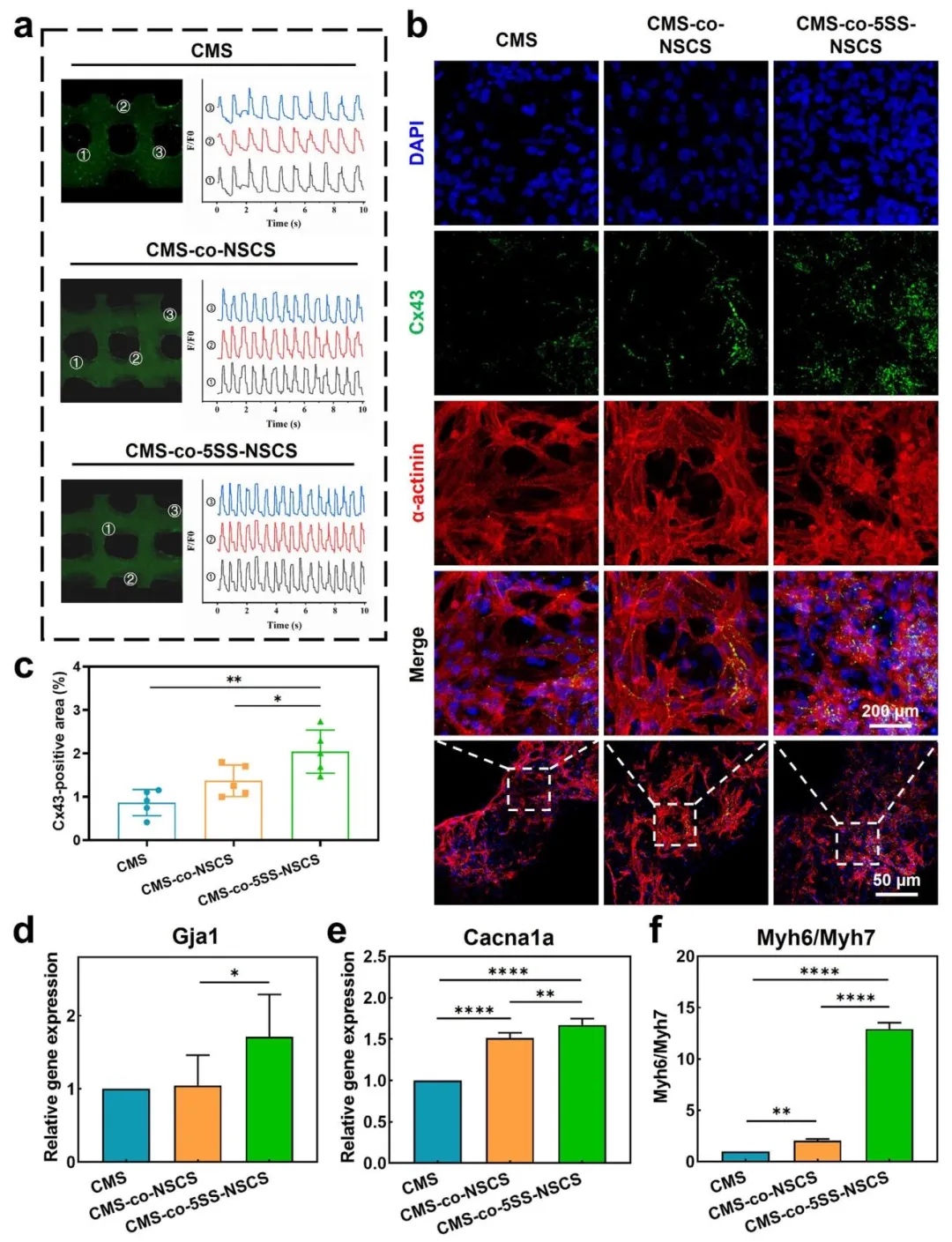
4. 预神经化支架对心肌构建体的体外作用,通过钙瞬变实验、免疫荧光染色和基因表达分析,研究了预神经化支架与心肌细胞共培养时的功能调控。结果显示,5SS-GelMA-NSC支架显著增强心肌细胞搏动同步性(钙信号同步化)、连接蛋白Cx43表达及收缩相关基因(Myh6/Myh7)活性,促进心肌结构成熟。
图4. 3D打印心肌细胞负载支架与神经干细胞负载支架共培养的心肌细胞活性表征。
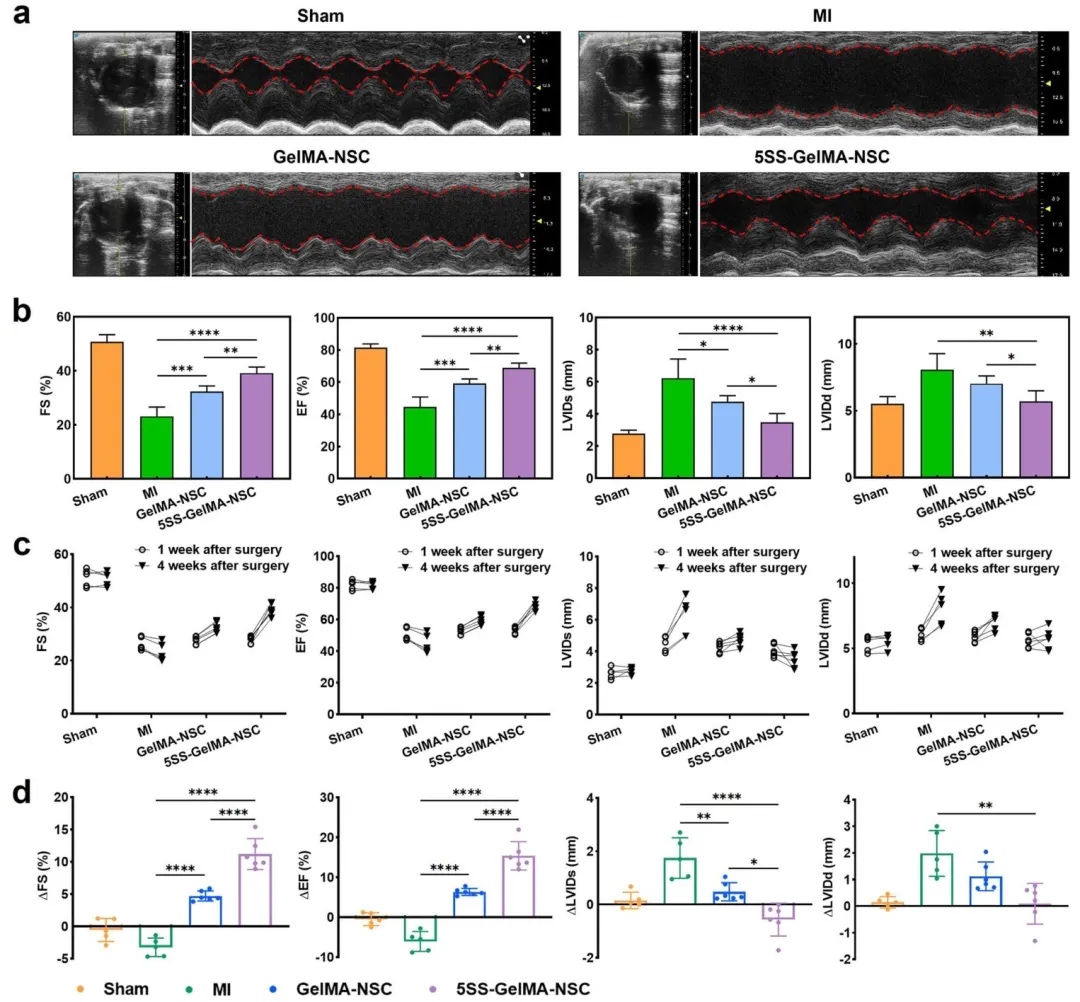
5. 预神经化支架的体内心肌修复效果,利用大鼠心肌梗死模型、超声心动图和组织染色(Masson’s Trichrome、WGA等),评估了支架植入后的心脏功能及组织修复。结果表明,5SS-GelMA-NSC组大鼠左心室射血分数(EF)和缩短分数(FS)显著提升,梗死面积减少,心肌细胞肥大减轻,且促进血管新生(vWF+和α-SMA+血管密度增加)。
图5. 支架移植后大鼠心脏功能评估。
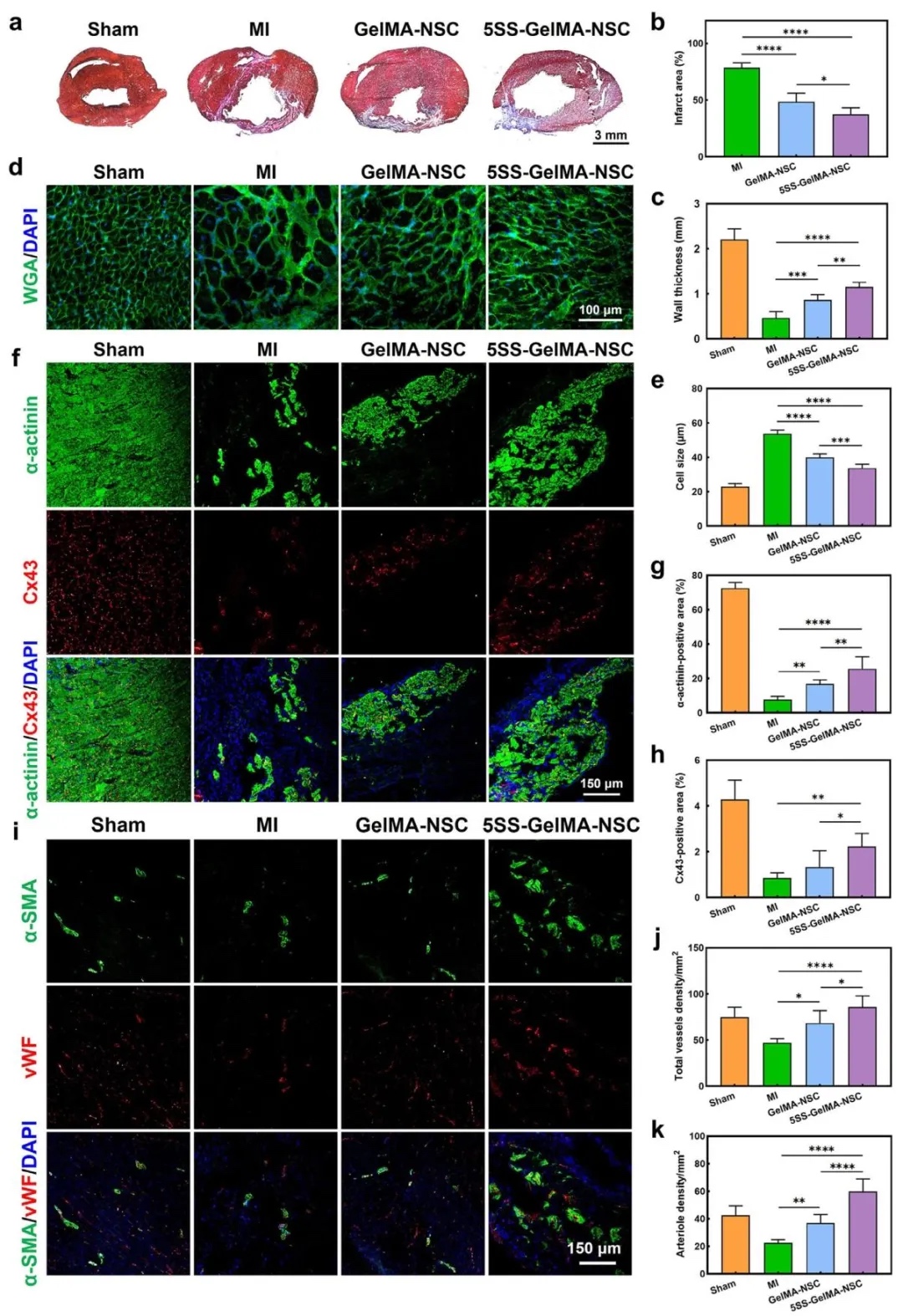
6. 心肌损伤修复的组织学观察,通过Masson’s Trichrome染色、小麦胚芽凝集素(WGA)染色和免疫荧光染色,研究了支架植入4周后大鼠心肌梗死区域的组织结构修复。结果显示,5SS-GelMA-NSC组梗死区域纤维组织比例最低,左心室壁厚度最大,心肌细胞代偿性肥大显著缓解,且Cx43、α-actinin等心肌功能相关蛋白表达升高,血管密度增加。
图6. 支架移植4周后大鼠心脏梗死区域的组织学表征。
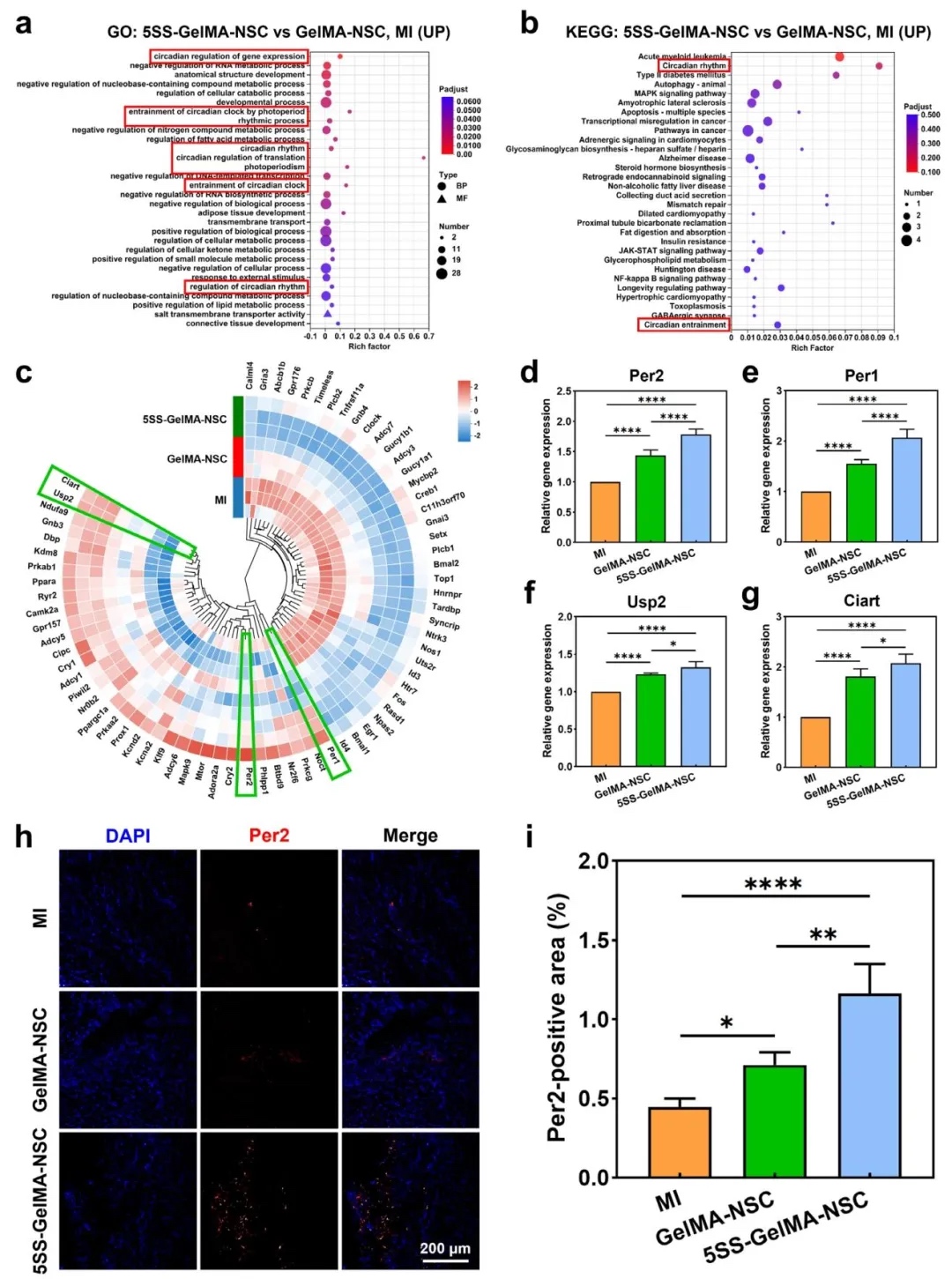
7. 预神经化支架的修复机制,通过转录组测序和基因表达验证,分析了支架诱导心肌修复的分子通路。结果显示,5SS-GelMA-NSC激活昼夜节律相关基因(Per2、Per1、Usp2、Ciart),其中Per2蛋白表达显著升高,可能通过调节炎症反应和血管生成促进心肌修复。
图7. 预神经化支架促进心肌修复的机制及昼夜节律相关基因和蛋白表达表征。
研究结论
本研究制备了由无机材料硅酸锶微粒子诱导的负载神经细胞的支架用于心肌梗死修复。硅酸锶微粒子通过释放适当浓度的锶和硅离子,调控神经干细胞的分化并促进神经元成熟,实现了负载神经干细胞支架的预神经化改造。在预神经化支架中,神经元无需人工信号引导即可促进心肌细胞功能修复梗死心肌,对受损心肌的结构恢复和功能重建效果显著。研究发现,预神经化支架似乎激活了四种与心脏保护相关的典型昼夜节律基因。基于神经调节器官昼夜节律的能力,推测含有神经元的预神经化支架可能通过影响昼夜节律相关基因的表达促进心肌梗死修复。因此,硅酸锶微粒子预神经化支架从昼夜生物过程角度激活了受损心肌的结构恢复和功能重建,为心肌梗死修复提供了一种有前景的策略。
文章来源:https://doi.org/10.1002/adma.202419765
(责任编辑:admin) |