3D��ӡ��Ϊ����Tϸ������������ˮ������ģ�IJ���
ʱ��:2024-10-16 08:54 ��Դ: EngineeringForLife ����:admin ���:��
| ϸ���������Ƶij���Ϊ�Կ���֢�������������ʹ�Ⱦ�������˸���Ч�IJ��ԡ�Ȼ������Щ������ص�ϸ�����������Ȼ�����Һ�ʱ�����������ǵ�Ӧ�÷�Χ����������ܰͽ�������PEG-����ˮ������֤���ܹ�����ʵ���ҹ�ģ�µ�ԭʼ����Tϸ�������� Ϊ�˽�һ���ƶ����ٴ�Ӧ�ã����������������������δ�ѧ(UAB)�����о���(ICMAB-CSIC)��Judith Guasch���Ŷ������������չ�ԣ���ͨ��3D��ӡ�ɹ�ʵ�֡���ˣ������ܹ����ԭʼ����Tϸ����������PEG-����ˮ�����еĽ���������ͬʱ����Ӫ�������������Ĵ��䣬�Ӷ��ڱ��ֱ��͵�ͬʱ�����ԭʼ����Tϸ������ֳ�ʡ���ˣ�����������Ľ�ϸ�������Ʒ�������ϸ����Ʒ�����Ҫ��������һ������ع�������Ϊ��3D Printing as a Strategy to Scale-Up Biohybrid Hydrogels for T Cell Manufacture�������·�����2024��09��16�յ��ڿ���ACS Applied Materials & Interfaces���� 
1.�������о����� 3D��ӡ����ͨ����㷽���Զ������츴�ӽṹ��3D���壬��Щ�ṹ���о�ȷ��Ƶļ�����״���ڲ�ͬ���͵�3D��ӡ�����У���������ӡ������ҽѧ�����������У���Ϊ���ذ���ͨ�����켷�����ϲ�������˿״��ʽ������ƽ̨�ϣ����γ�3D�ṹ��Ϊ���������˹��ܰͽ᷽����ǰ����һ�����������˷���ǰ�����������Tϸ��������ص�ACT���ƣ�֮ǰ������PEG-����ˮ������������Ϊ3D��ӡ��īˮ������������Tϸ��������ͼ1���� 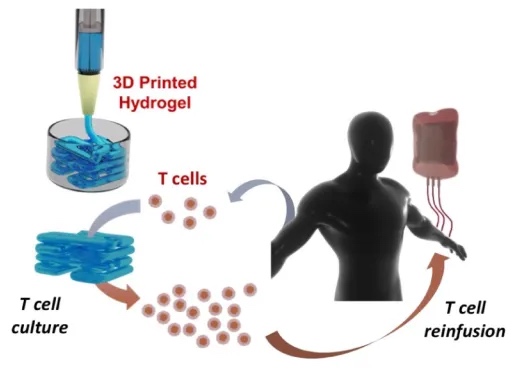
ͼ1 ʹ��3D��ӡˮ��������ϸ������������Tϸ����Ʒ�������
��PEG-����ˮ������Ϊ3D��ӡ��īˮ�� Ϊ���Ż�Ӫ��������ͷ��サ���������ϸ������ʺ���ֳ��ѡ����3D֧����ơ�����Ʊ�����ˮ�������е�����϶�ȣ�����Ч��֮ǰ�ѵõ�֤�������⣬ѡ����һ�ּ���ƣ�������Ƴ����������²��ϣ����IJ�������ɣ��������Ϊ1.5���ף�ͼ2A���������Ҳ��������ת��DZ���ͼ���ת��ѡ�Ϊ�ˣ�PEG-����ˮ������Ԥ�ȳ��Ͳ�������Ϊ3D��ӡ��īˮ���������ºͲ�ͬ��ˮ�����γ�ʱ����С�����������4Сʱ��4��PEG���������ǰ����ܻ��ĸ��������ﵽ���㹻��ճ�ȣ����Խ��д�ӡ��ͼ2B����Ȼ��������֧����ʾ��һ���Եͣ���ӡ�����е������ֻ�������Ϊ�������������Ԥ���͵�ˮ�����ڻ�Ϻ�12Сʱʹ�ã��õ����ʺϱ���Ŀ�ĵ�֧�ܣ�ͼ2C��������Ļ������˽�PEG-����ˮ�����ܽ���ϸ���������н���DZ����ϸ��ʵ��Ŀ����ԡ�����������£�ˮ�������γ��������������������ڴ��ڽ��ٵĶ������ӣ���ٽ��˶�������γɣ��Ӷ������˿�����ˮ�����γɵ�����Ȥ���ǣ����ò��Ͽ��Ժ����ش�ӡ��ͼ2D���� 
ͼ2 Ϊ�Ż�PEG-����ˮ������3D��ӡ����Ƶ�֧��ʾ��ͼ
��PEG-����ӡ��֧������CD4+ Tϸ�������� һ��֤����PEG-����ˮ�����Ŀɴ�ӡ�ԣ��ʹ�ӡ��������3D��״�ṹ��Ϊ������CD4+ Tϸ��������3D֧�ܡ���Ϊ��㣬ʹ��Լ35��50�˵IJ��ϣ��ֱ���������4���6����ɵ�֧�ܣ�ÿ����֮��ļ��Ϊ1.5���ס�Ȼ����ÿ����106��ϸ����Ũ�ȣ���������CD4+ Tϸ���������������棬����6�졣���ţ�ͨ����ʽϸ�����������Ʒ�Ͷ��գ�����������ϸ��������ֳ�����ƺ�����ָ����32���������бȽϣ���ͼ3A�CC���� ����һ���У��������������͵�3D��ӡˮ�����ڽ��ֺ�5�������Tϸ���ı��͡��ر��ǣ�ϸ��������Ϊ��ʼ�ͣ�TN��CD45RO-/CD62L+�������ļ����ͣ�TCM��CD45RO+/CD62L+����ЧӦ�ͣ�TEFF��CD45RO-/CD62L-����ЧӦ�����ͣ�TEM��CD45RO+/CD62L-���������IJ�ˮ������ͼ3D�����۲쵽TCM���͵İٷֱ��������ӣ�ͬʱTEM���١�������˵���IJ��ӡˮ������TCM��λֵΪ66%�����Զ���Ϊ61%�������Զ���Ϊ45%�����⣬��ӡ֧�ܵ�TEMƽ��ֵΪ23%�������Զ��յ�30%�����Զ��յ�14%��ȡ����TNϸ����ʧ��ϸ����39%�������ٵ�����������ʹ��ˮ����������ϸ����5%��6%�����ܼ���ϸ��֮��û�л���������졣���ܶ�������֧��Ҳ�۲쵽�����Ƶ����ƣ����۲쵽�IJ��첻̫���ԣ��ر��Ƕ�TCM���Ͷ��ԣ�ͼ3E���� 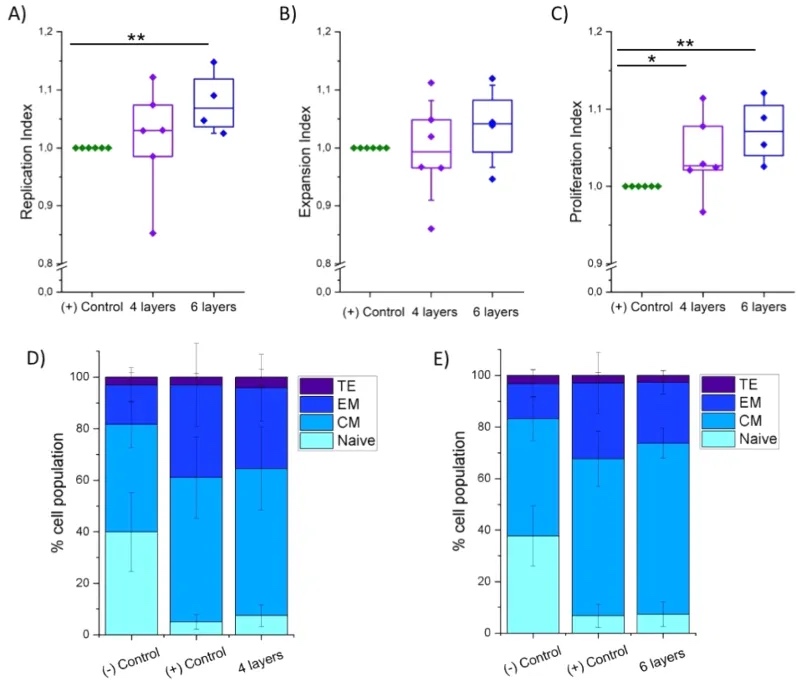
ͼ3 �ڴ�ӡ��PEG-����ˮ����������6��ij�������CD4+ Tϸ���ı�����ֳ�����ˮ�����߶�Ϊ4���6�㣬�Լ��������������Զ��գ�
��ͨ��3D��ӡ��������ˮ�����ijߴ硿 ������о��Ѿ�֤����ʹ��PEG-����ˮ�������Ը�������ϸ��������Ч����������ֳ�ͷֻ����������ACT��ϸ���Ʒ���˵����Ȥ�Ľ����Ȼ������Щ������Ҫ����������ܴﵽ������������Ŀǰ�Ľ�����ڲ���1�����������ȡ�õġ���ˣ��б�Ҫ����ˮ�����ijߴ���ʵ�����ٴ�Ӧ�á����ǣ�֧�ܳߴ�����ӿ϶���ʹϸ����Ӫ�����ʺ�����Ĵ���������ѡ�Ϊ�˽��������⣬�����о���ʹ��3D��ӡ����������֧�ܳߴ�ķ�������ˣ�����ѡ����һ��ֱ���������ͷ��25G�����Ƚ�������֮ǰ����ͷ�Ŀɴ�ӡ�ԡ�������������£�ͨ����Ԥ���γɵ�PEG-����ˮ����ͨ����ͷ��������ӡƬ�Σ��������������ά��ͼ4A, B�����籾����Ԥ�ڵ�������ʹ�ø�����ͷ�õ�����άֱ���������ӣ�ͼ4C���� 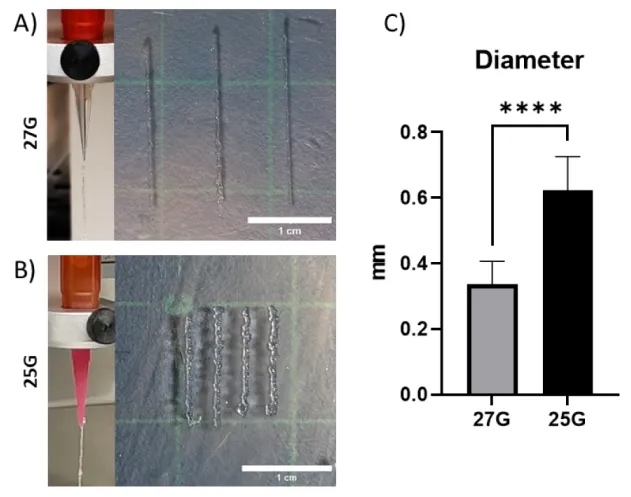
ͼ4 �ڿ����м�����ˮ��������27G��25G��ͷ��ӡ����ά�Ĵ���ͼ��
���⣬��ɢ��Ҳ��1.68 �� 0.35��27G�����ӵ�2.49 �� 0.41��25G��������������¶��ǿ��Խ��ܵģ���Ϊ���Ƕ���1��3֮�䡣��33�����⣬ͨ�����һ����ʮ����ɵ�Բ������ṹ��ÿ��֮����������Ϊ1.5���ף����Խ���ķ�ʽ��ֱ���У��Խṹ�������ģ�ͼ5A�������������ʹ�����ܹ�����ӡ���ϵ���������10����Ϊ�˽�һ����������ƣ����IJ���X����������ϲ�ɨ�����ͻ���ɨ�����������SEM����������ӡˮ�����Ŀ��ͻ����ԣ�ͼ5B, C��������ͼ����ʾ�����Կ����ֲ�ṹ�Լ�֮ǰ�ڴ��ˮ�����й۲쵽��ˮ�����ڲ��ṹ�� 
ͼ5 Ϊ���֧�ܳߴ����Ƶ�3D��ӡˮ������ʾ��ͼ����Ƭͼ����ֱ��Ϊ1���ף��Լ����ò��ϵ�����
���⣬ͨ������ѧ������֧�ܵĻ�е���ܣ�ͼS3��������δ��ӡ���Ͻ����˱Ƚϡ���ӡˮ�����Ĵ���ģ����G�䣩Ϊ447 �� 34 Pa����δ��ӡˮ�����Ĵ���ģ��Ϊ1.1 �� 0.1 kPa����Ԥ�ڵ�����������ˮ�����е���ͬ������ȣ���ӡˮ�����ڴ�ӡʱʧȥ�˲���Ӳ�ȡ�Ȼ��������ˮ�������͵Ļ�е�����ǿɱȵģ���ӡ��ˮ�����ṩ�˸��õ�ϸ����������ڲ��Ŀɼ��ԣ�����ˮ������ȣ��ṩ�˸��õĻ������������ֲ��ϵ�ʹ�ù�ģ�������3D��ӡˮ��������������ԭ������CD4+Tϸ����ͼ6����Ϊ��ȷ����ӡ�ṹ�����ƣ����Ľ��������ͬ������δ��ӡ��ˮ���������ṹ�������˱Ƚϡ� 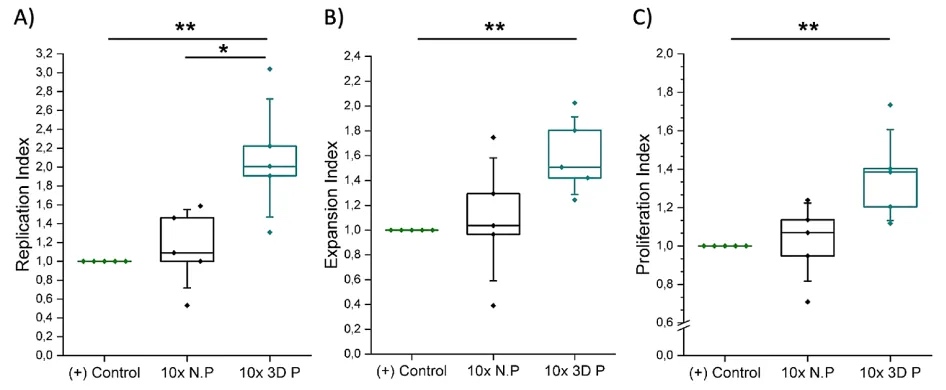
ͼ6 �ڲ��ֺ�6�죬���������ij�������CD4+ Tϸ�������Զ��գ������Ǵ�ӡPEG-����ˮ������10x N.P���ʹ��3D��ӡPEG-����ˮ������10x 3D P���ı�����ֳ���
2.�ܽ���չ�� ����֤����PEG-����ˮ�������Գɹ�����3D��ӡ����Ϊ������ϸ���ṹ���ڵ��ڶ�DZ��Ӧ�ô��˴��š����⣬������������ȣ��ڴ�ӡ֧���з�����ԭʼ����CD4+ Tϸ������ֳ�õ�����ǿ��6��֧�ܵ���ֳ�ʸ����IJ�֧�ܡ����⣬��Щ3D��ӡ��ˮ�����ڵ�5��ʱ������TCMϸ���İٷֱȣ�����һ�����������Ƹ�Ч����صı��͡���������˴���3D��ӡˮ����������PEG-����ʵ����ˮ�����Ŀ���չ�ԣ���ˣ�������ΪACT���������ϸ��������3D֧�ܵ�DZ����;������Щʵ���У������Ƚ�����������������ˮ������ȣ�3D��ӡˮ��������˸��ߵ���ֳ���ʡ���Щ�������ͨ��3D��ӡˮ����������ˮ������ȣ�ϸ�������Ӫ�����������ڲ��������ǿ�����͡���ˣ�����չʾ�˽�����������3D��ӡ�����������ϣ����ܲ������ٴ������õ�PEG-����ˮ������ (���α༭��admin) |
- ��һƪ��Incodema3D�����EOS������ͨ������3D��ӡ������չ���պ���������ģ
- ��һƪ������ȥ������֧�ŵ�4S����3D��ӡ����