悉尼大学利用3D打印构建血管模型
时间:2024-09-24 09:09 来源:EngineeringForLife 作者:admin 点击:次
血栓形成是心血管疾病(CVDs)的主要驱动因素,导致了全球范围内的高发病率和死亡率。然而,当前用于研究血栓形成的动物模型和体外系统存在局限性,无法充分模拟人类复杂的血管结构和血液动力学条件。这些限制阻碍了对血栓形成机制的深入理解,以及新治疗方法的开发。生物打印技术作为一种新兴的方法,展现出构建结构和功能上模拟天然血管的生物模拟血管模型的潜力。通过精确控制细胞、生长因子和生物材料的三维空间排列,生物打印能够制造出具有复杂结构的定制化组织构造,为血栓研究提供了新的平台和可能性。
鉴于此,悉尼大学Lining Arnold Ju等人综述了生物打印技术在血栓研究中的应用,强调了血栓形成作为心血管疾病主要原因的重要性,并指出了传统研究方法的局限性。文章探讨了生物打印如何模拟血管的结构和功能,以及如何通过精确的空间排列细胞和生物材料来构建复杂的血管模型。讨论了生物打印技术的最新进展,包括多材料打印和微流体集成,这些技术有助于开发更符合生理条件的血栓模型。同时,文章也提出了生物打印领域面临的挑战,如开发更先进的生物材料和标准化打印流程。 1.主要内容 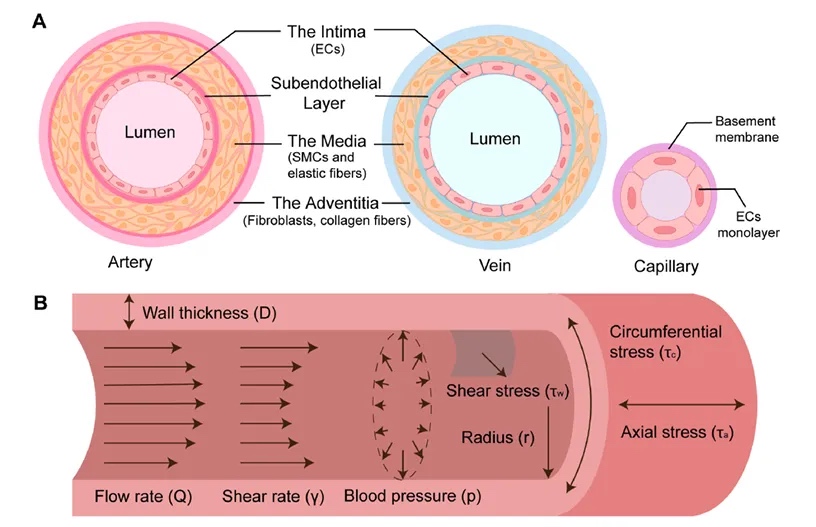
图1 血管壁结构和机械力
它展示了动脉、静脉和毛细血管的血管壁结构,这些血管壁由三层组成:内膜、中膜和外膜。内膜由内皮细胞(ECs)构成,中膜包含平滑肌细胞(SMCs)和弹性纤维,而外膜主要由胶原纤维构成。此外,还描述了血管所承受的主要机械力量,包括剪切应力、周向应力和轴向应力。剪切应力是血液流动对血管壁的摩擦力,受流量、剪切率、流体粘度和血管腔半径的影响。周向应力是作用在血管壁切线方向上的力,而轴向应力是沿血管纵向轴施加的力。这些力量对血管内皮细胞的功能和血管稳态起着重要的调节作用,剪切应力的变化可能导致内皮细胞功能障碍,进而影响血栓形成的过程。 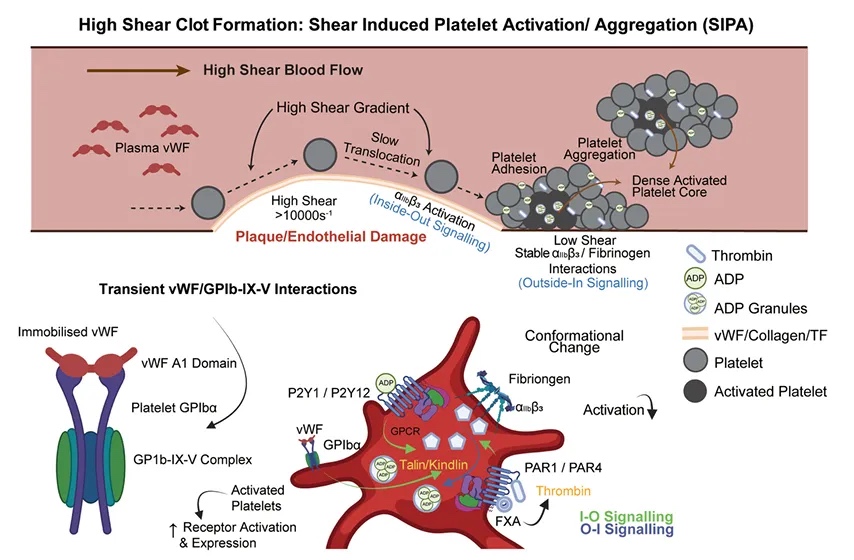
图2 剪切诱导的血小板激活/聚集
剪切力诱导的血小板激活/聚集(SIPA)是血小板对血流剪切力的生物学响应,通常发生在血液流经狭窄处或高剪切率条件下。这一过程涉及血管性血友病因子(vWF)的释放、血小板形态和受体结合的变化、血小板聚集以及细胞内信号通路的激活。在高剪切力下,血小板GPIb与vWF之间的相互作用启动了血小板的粘附和激活。激活的血小板释放多种激动剂,如腺苷二磷酸(ADP)和血栓素A2(TxA2),这些激动剂进一步放大血小板聚集和血栓形成。 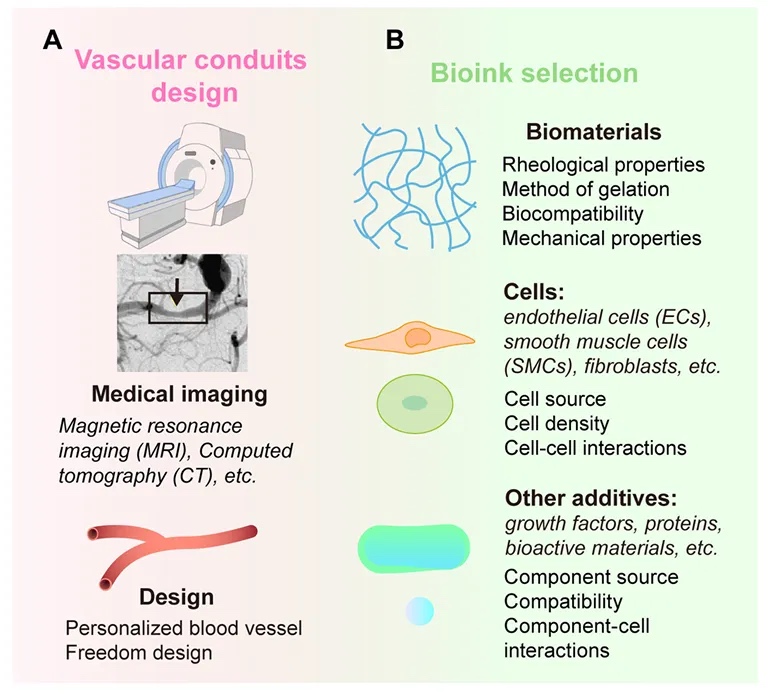
图3 生物打印血管导管的制备
首先,通过使用MRI、CT和其他医学成像技术,可以获得血管网络和细胞的结构、尺寸和空间排列的详细信息,这对于设计患者特异性的血管通道至关重要。其次,选择适合生物打印的生物墨水,这些生物墨水通常由具有适当流变学和机械特性的水凝胶组成,以确保成功的生物打印。细胞的选择同样重要,例如,可以选择内皮细胞(ECs)、平滑肌细胞(SMCs)和成纤维细胞来准确复制天然血管的结构和功能。此外,生物墨水中的生物活性成分也是确保打印性、结构完整性以及支持细胞生长和功能的必要因素之一。 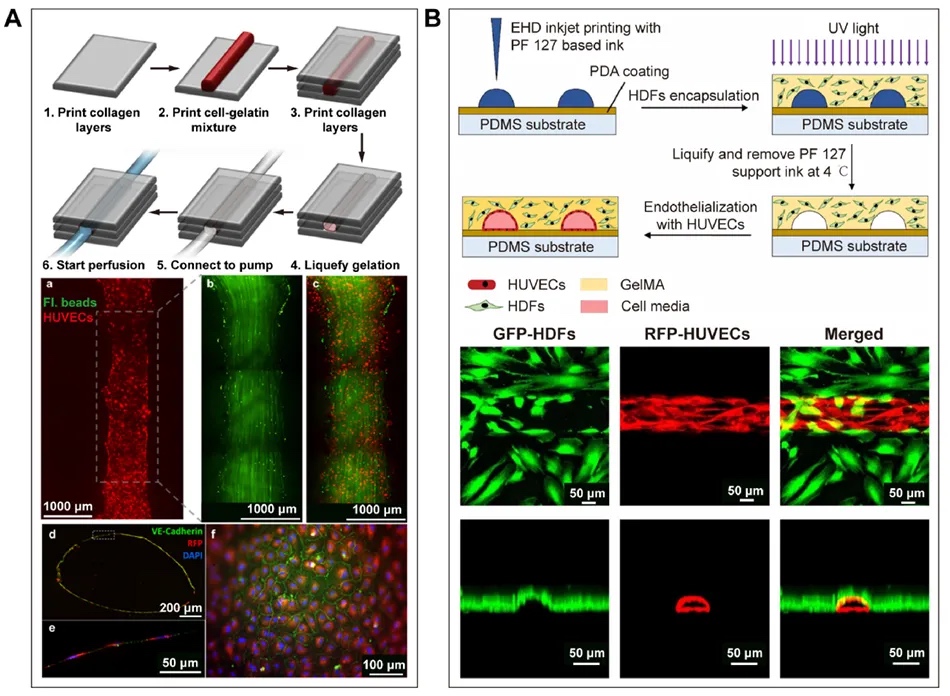
图4 喷墨式生物打印用于制造血管结构
(责任编辑:admin) |