3D打印复合支架促进骨形成和血管化
时间:2024-08-16 10:27 来源: EngineeringForLife 作者:admin 点击:次
| 骨缺损治疗的支架应支持血管化和促进骨形成,以促进转化为生物医学设备应用。目前用于骨缺损治疗和骨再生的生物材料支架迫切需要改进,以增强组织整合、血管化和骨形成,同时最小化材料的复杂性。但传统支架在提供足够的通道结构以有效的营养供应和废物清除方面往往面临限制,因此含有通道的生物材料支架已经成为一种潜在的解决方案。基于此,澳大利亚莫纳什大学Neil
R. Cameron、Mikaël M.
Martino提出了一种新方法,利用3D打印水溶聚乙烯醇(PVA)牺牲模具,设计具有微通道和多尺度孔隙率的聚合高内相乳液(polyHIPE)支架。使用熔融沉积模型生成两个牺牲模具变体(250
μm和500
μm),填充HIPE,随后溶解以生成含有微通道的polyHIPE支架。体外评估显示,细胞浸润、增殖和成骨分化显著增强,强调微通道对细胞行为的良好影响。成骨因子BMP-2实现较高的负载效率和可控释放,微通道促进生长因子的释放。对小鼠临界大小的颅骨缺损模型的评估显示,在含有BMP-2的微通道支架中,血管化和骨形成增强。综上,本研究不仅介绍了一种在polyHIPE支架中创建多尺度孔隙率的可行方法,而且强调了其增强细胞浸润、控制生长因子释放和体内性能的能力。以上发现表明,polyHIPE支架在骨组织工程和再生医学中有很好的应用前景,并有望促进这类生物材料支架的转化。 相关研究内容以“Bioactive Polymer Composite Scaffolds Fabricated from 3D Printed Negative Molds Enable Bone Formation and Vascularization”为题于2024年7月30日发表在《Acta Biomaterialia》。 
图1 含微通道的多孔DPEHA支架制备
PVA细丝的3D打印产生在水平面上0、90度观察到层状垂直支柱,支柱直径分别为250 μm和500 μm(图1A)。在高内相乳液(HIPE)紫外光聚合、负模溶解和支架脱水之后,由此产生的微通道穿过垂直轴和水平轴上在整个支架相互连接(图1B)。SEM图像显示,两个支架通道表面上有小开孔,直径为250 μm(250μC)和500 μm(500μC)的微通道。 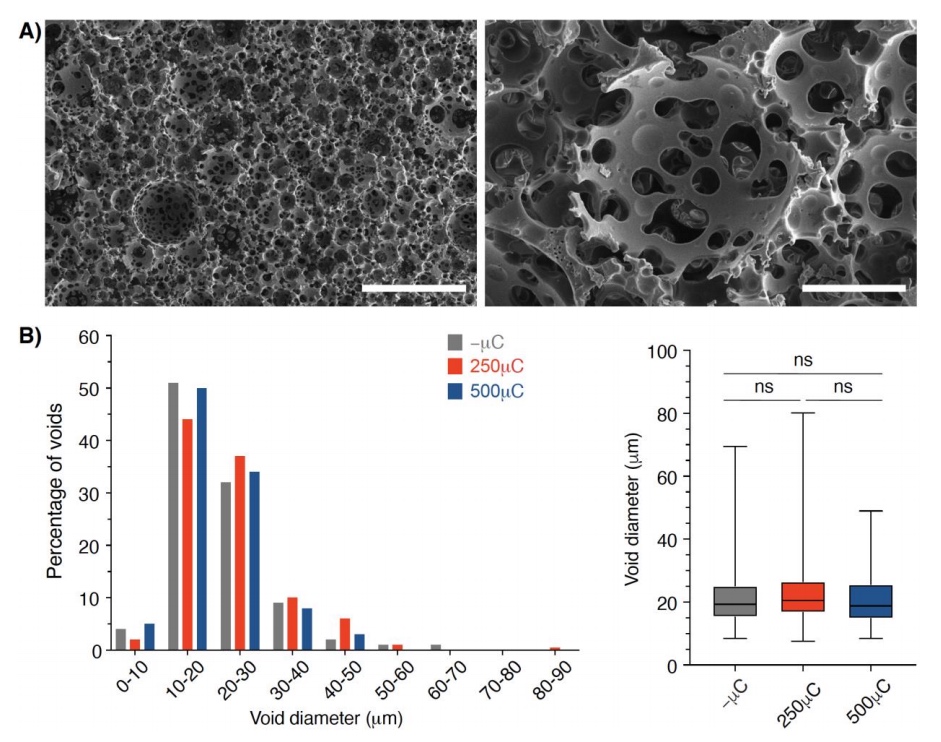
图2 多尺度孔隙度DPEHA polyHIPE支架的形态学特征
PolyHIPE材料的形态学特征在所有三种支架变化中都很明显,如圆形和清晰的孔隙(图2 A)。对支架材料孔径直径的测量表明,所有材料的孔尺寸都相似且正偏态分布,表明牺牲模板对内孔隙直径的分布没有显著影响(图2B)。 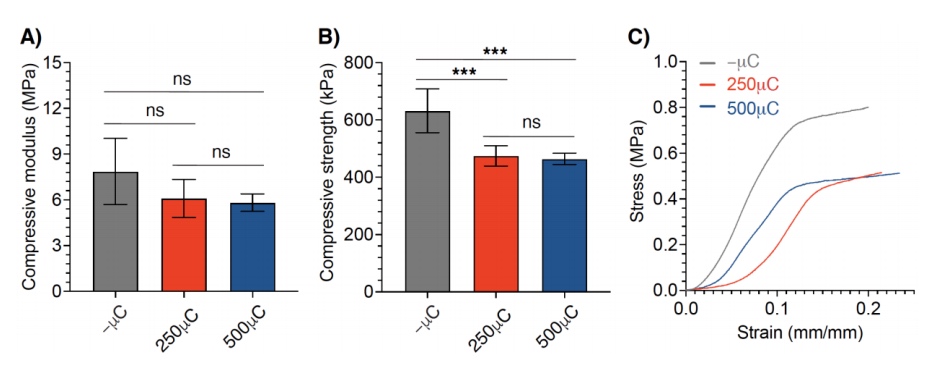
图3 含/不含微通道的DPEHA polyHIPE支架的力学表征
支架的压缩模量、极限压缩屈服强度和应力-应变曲线的测量值如图3所示。结果显示,-μC、250μC和500μC支架之间的压缩模量没有显著差异(图3A)。与非通道材料相比,250μC和500μC支架的极限抗压强度均显著降低(图3B)。所有支架变化的应力-应变曲线均显示出韧性材料具有相当大的弹性变形特征(图3C),其J形非线性曲线代表polyHIPEs和其他生物材料的拉伸试验应力-应变曲线。250μC和500μC支架在给定的应变值下均表现出较低的应力值,表明随着在材料中引入微通道,机械响应发生改变。 
图4 多尺度孔隙度DPEHA polyHIPEs支架的体外评价
为了研究支架中的微通道是否能增强细胞在生物材料内部的迁移和定植,本研究将MG63骨肉瘤细胞接种到支架表面,培养长达28天(图4A)。H&E染色显示,与非通道支架相比,细胞浸润到更多的内部区域;相反,在没有通道的支架中,只有少数细胞浸润到靠近支架表面的空隙中(图4B)。SEM证实在单个通道内存在细胞,并观察到密集的ECM层在通道表面和空间上扩散(图4C)。用刃天青还原试验测定支架培养4周后,支架中的细胞活力和增殖情况(图4D)。结果与组织学结果一致,支架在整个培养期间均表现出高活力。 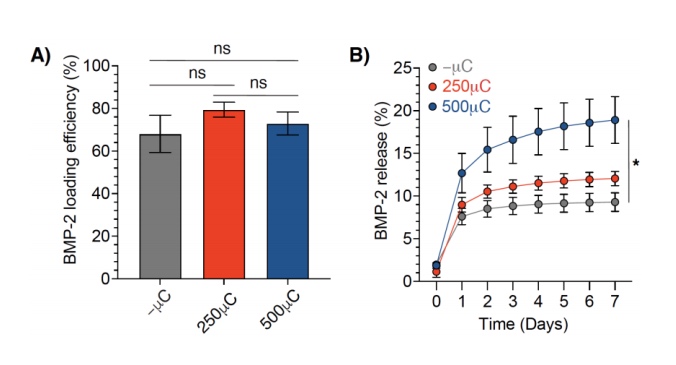
图5 DPEHA polyHIPE支架中BMP-2的负载效率和累积释放谱
接下来,本研究探索了负载BMP-2的polyHIPE支架的加载和释放,以估计植入后可能发生的释放谱。在所有支架中均观察到相对较高的加载效果,-μC、250μC和500μC通道支架的负载效率无显著差异(图5A)。在最初的24小时内,所有的支架均表现出总负载BMP-2的低突发释放,500μC支架的BMP-2累积释放百分比最高,其次是250μC,-μC支架的释放谱最低(图5B)。 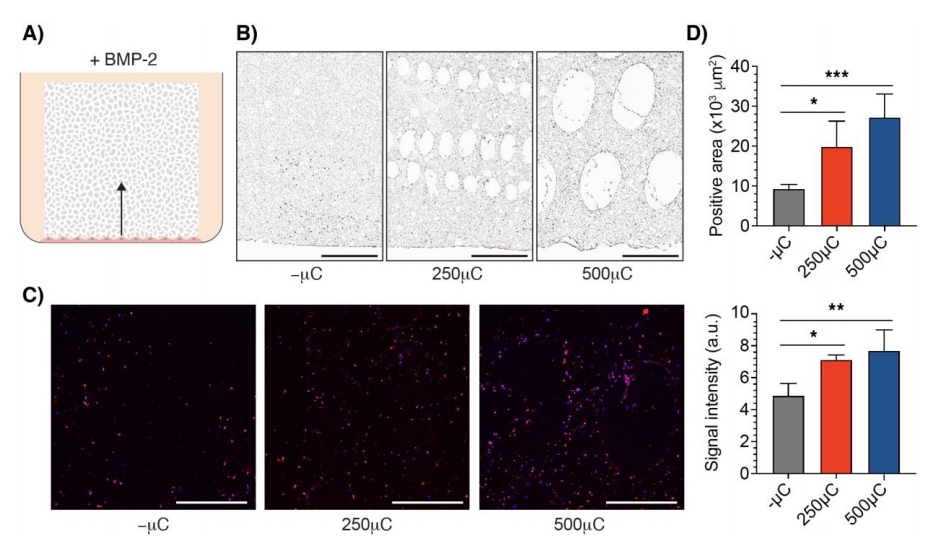
图6 微通道DPEHA polyHIPE支架中MSC的浸润和成骨分化
微通道PolyHIPE支架沉积在MSC单层上,将细胞在含有BMP-2的成骨分化培养基中培养3周(图6A)。在培养的第21天,H&E染色显示,与非通道PolyHIPE支架相比,微通道PolyHIPE支架中的细胞浸润到更多的内部区域(图6B)。此外,通道支架中较高的细胞浸润翻译较高水平的晚期成骨细胞分化标志物骨钙素(图6C、D)。 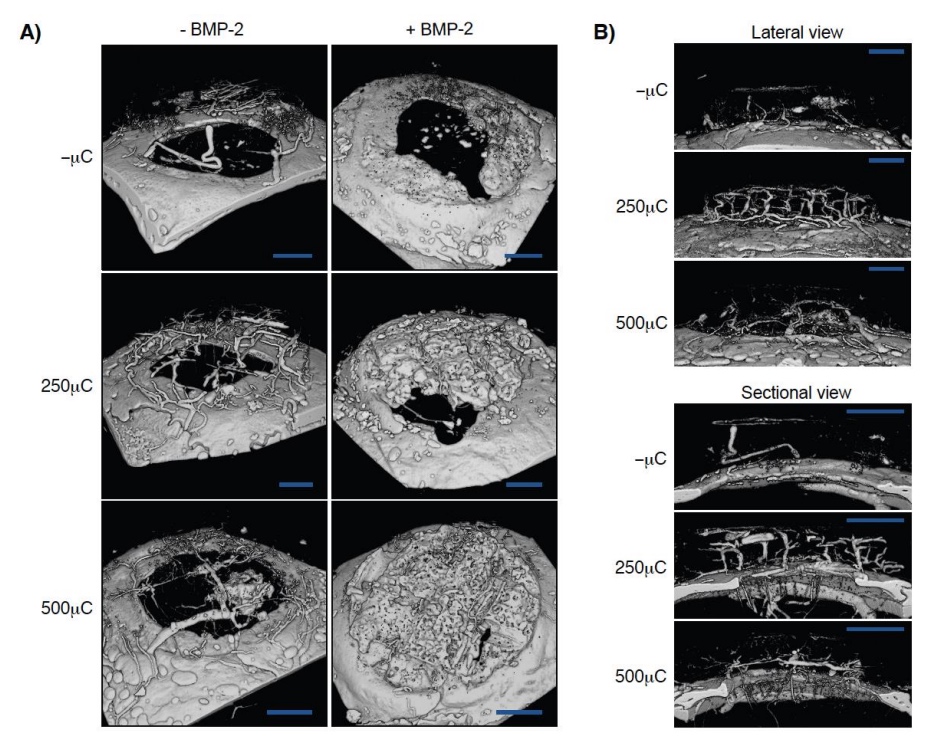
图7 DPEHA polyHIPE支架植入颅骨缺损的血管化研究
本研究通过微注射MV-122,结合高分辨率X线CT,观察牺牲模板polyHIPE支架获得的三维血管网络。血管包围非负载支架的表面并靠近上下表面,包围了polyHIPE支架的侧面。-μC/-
BMP-2支架的血管主要在支架外表面。相比之下,250μC/-BMP-2和500μC/-BMP-2支架在整个支架上都有广泛的、相互连接的血管浸润(图7A、B)。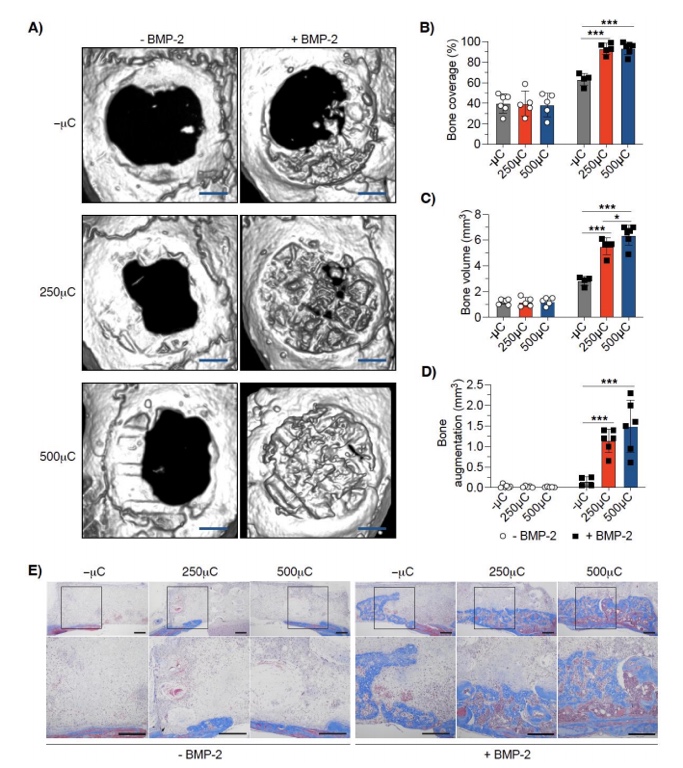
图8 微通道DPEHA polyHIPE支架诱导骨形成的定量研究
接下来,用较低分辨率(20 μm)的显微CT扫描植入物,以量化支架诱导的新骨生长(图8 A)。在没有BMP-2的支架中,非通道组和通道组在缺损覆盖、新骨总体积和垂直骨增加方面没有显著差异,而所有BMP-2组均表现出更大的缺损覆盖范围和更多新骨形成(图8B、D)。此外,与通道较小的支架相比,通道较大的支架骨形成显著增加(图8C)。与有BMP-2但没有微通道的支架相比,有BMP-2和微通道的支架的骨增强量增加近10倍(图8D),表明微通道显著促进新骨形成。然后对颅骨组织进行组织学处理,用Masson染色以进一步检查polyHIPE支架内的新骨形成和细胞浸润(图8E)。 全文小结 综上所述,本研究将乳剂模板与可提取的3D打印结合,制备了用于骨组织工程的具有多孔孔隙度的聚合物支架。所得到的支架有一个由乳化液模板产生的完全互联的微孔网络,以及一个直径为250或500 μm的相互连接的网状微通道网络。在体外,骨肉瘤细胞(MG63)能够更好地穿透微通道支架并填充支架内部。同样,骨源性MSCs可以从单层培养向上迁移到非通道支架中,增殖并显示成骨标记物。小鼠颅骨缺损模型结果表明,当添加骨诱导因子BMP-2时,微通道支架的骨诱导作用更大,以及微通道支架促进血管化。在500μm+ BMP-2中,8周后颅骨缺损几乎完全闭合。总之,本研究结果表明,乳剂模板和负模通道的结合产生了很有前途的骨组织工程支架。 文章来源: https://doi.org/10.1016/j.actbio.2024.07.038 (责任编辑:admin) |