爱丁堡大学开发3D打印人工血管,用于改善心血管疾病治疗效果
时间:2024-07-30 09:58 来源:南极熊 作者:admin 点击:次
2024年7月29,来自爱丁堡大学与赫瑞瓦特大学的研究人员利用一种名为混合挤压打印和电纺丝技术开发了新型3D 打印血管,旨在取代目前手术中使用的人体和合成静脉,用于改变血液流动路线。

△3D 打印血管。图片来源:爱丁堡大学 Norbert Radacsi 博士。
这项研究以题为“Fabrication of a Compliant VascularGraft Using
Extrusion Printing and Electrospinning
Technique/利用挤压打印和静电纺丝技术制造顺应性血管移植物”的论文发表在《Advanced Materials
Technologies》期刊上。

相关论文链接:https://onlinelibrary.wiley.com/doi/10.1002/admt.202400224
心血管疾病仍然是全球主要的死亡原因,因此小直径血管移植物在治疗心血管疾病方面需求量很大。最突出的心血管疾病包括冠状动脉疾病、外周动脉疾病和腹主动脉瘤。通常进行血管重建手术(或搭桥手术),使用血管导管重新引导受影响或阻塞动脉周围的血流。自体移植物,例如隐静脉、乳内动脉和桡动脉,仍然是搭桥手术的黄金标准,但失败率很高,并且移植物采集经常导致供体部位发病率。此外,这些自体移植物在尺寸或机械性能方面很少是最佳的。大多数由合成材料(例如
Dacron 和 ePTFE)制成的市售移植物适用于大直径动脉(>6
毫米)。然而,当用来替代小直径动脉时,它们常常会因感染和内膜增生而失败。
为此,爱丁堡大学开发了一种制造双层血管移植物的新方法。研究人员采用了一种混合生物打印和静电纺丝装置,制造出来表现出接近天然动脉的生物力学特性的分层移植物。
据爱丁堡大学称,3D 打印血管与人体静脉的特性非常相似,有望彻底改变心血管疾病的治疗方法。这些坚固、柔韧、凝胶状的管子采用新型 3D 打印技术制造而成,可以取代目前手术中用于改变血流方向的人体和人造静脉,从而显著改善心脏搭桥手术患者的治疗效果。
人造血管的开发有助于减少在搭桥手术中切除人体静脉时产生的疤痕、疼痛和感染风险,每年英国大约有 20,000 例此类手术。此外,这些产品有助于缓解小型人造移植物失败的风险,因为这些移植物很难融入人体。
在人工血管的制造过程中,爱丁堡大学工程学院领导的研究小组利用集成在 3D 打印机中的旋转主轴,从水基凝胶中制造出管状移植物。然后使用静电纺丝技术对打印的移植物进行加固,静电纺丝技术利用高压拉出非常细的纳米纤维 - 将可生物降解的聚酯分子包裹在人造血管中。机械性能和生物性能测试表明,最终产品与天然血管一样坚固。

△图1
纤维增强型 gelMA 移植物制造概述。a) 纤维增强型 gelMA 结构制造步骤示意图。b) 混合印刷和电纺装置。c) 全长血管移植物。d)
电纺纳米纤维增强型制造的 gelMA 移植物(比例尺:15 毫米)。e) 使用镊子完全压缩的移植物(比例尺:2 毫米)的自发荧光图像,f)
移除镊子上的力后完全恢复的移植物结构(比例尺:2 毫米)。g) 制造的血管移植物横截面的数字图像,显示内部 gelMA
层和外部电纺纤维层(比例尺:0.4 毫米)。

△图2
血管移植物的爆破压力和柔顺性测量。a) 定制 Instron 3367 万能试验机的照片。b) 爆破压力测试的测试台。c)
爆破压力测试期间的纤维增强 gelMA 移植。d) 爆破压力测试后移植失败。e) 移植柔顺性测量装置的示意图。f) 柔顺性测量装置的照片。g)
柔顺性测试期间,在 150 mmHg 压力下由 75/25 PCL/PLCL 电纺纳米纤维增强的 10% gelMA 结构。

△图3
gelMA水凝胶的流变特性和纤维增强 gelMA 移植物的拉伸测试。a)26°C 下 gelMA 水凝胶的粘度随剪切速率的变化。b)22、24 和
26°C 下 7.5% gelMA 的粘度随剪切速率的变化。c) 26°C 下 gelMA 水凝胶的储能和损耗模量随角频率的变化。纤维增强
d) 7.5%、e) 10% 和 f) 12% gelMA 移植物的圆周应力-应变曲线。纤维增强 g) 7.5%、h)10% 和 i) 12%
gelMA 移植物的纵向应力-应变曲线。j) 纤维增强 gelMA 移植物的圆周方向杨氏模量。 k) 纤维增强 gelMA
移植物在纵向的杨氏模量。l) 纤维增强 gelMA 移植物周向强度。m) 纤维增强 gelMA 移植物纵向强度(***,p <
0.0001;**,p < 0.001;*,p < 0.05;NS,不显著)。
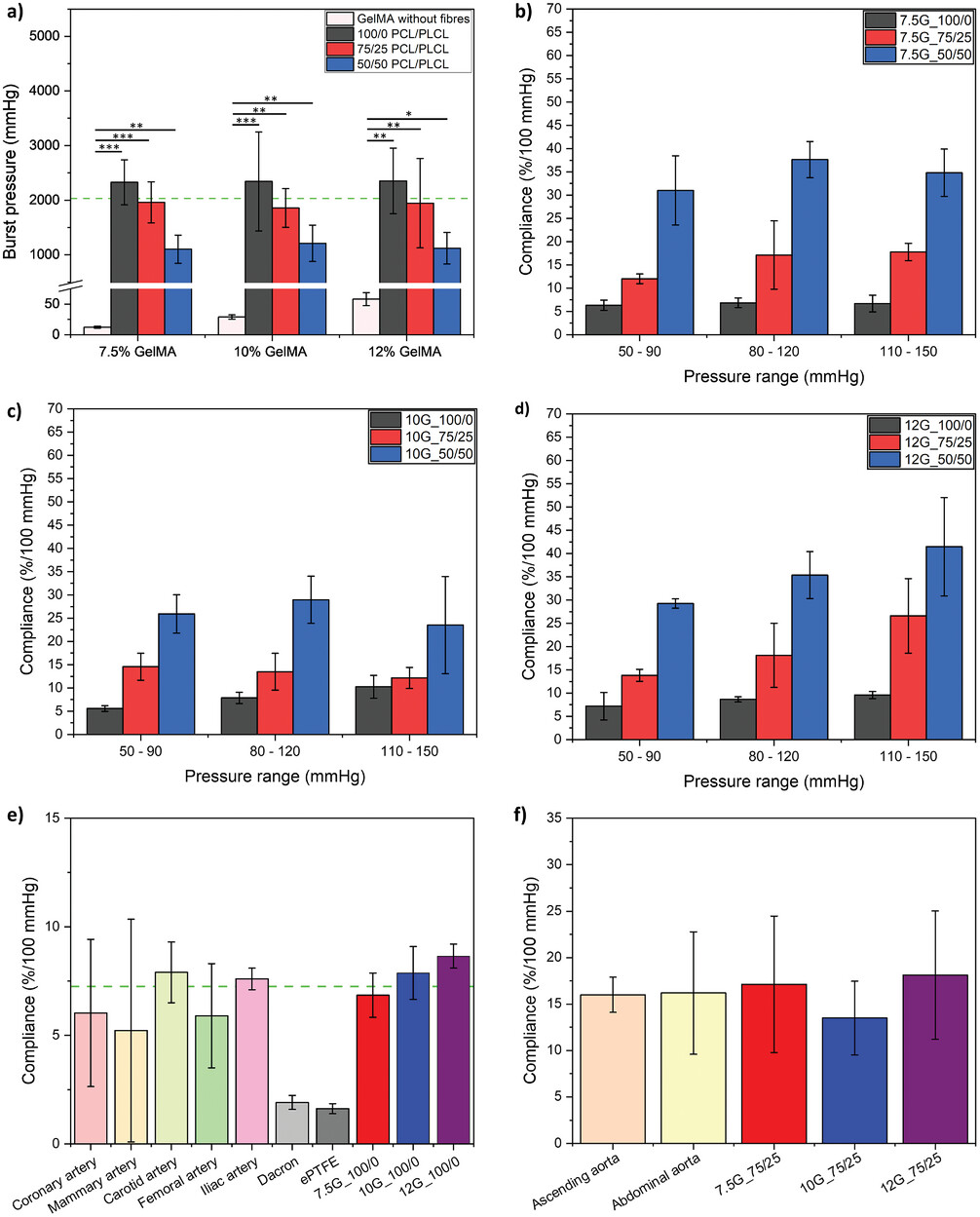
△图4 纤维增强 gelMA
移植物的爆破压力和顺应性数据。a) PCL/PLCL 纤维增强 gelMA
移植物的爆破压力,绿色虚线显示小直径动脉的平均爆破压力(***,p < 0.001;**,p < 0.01;*,p <
0.05)。b) 7.5%、c) 10% 和 d) 12% PCL/PLCL 纤维增强 gelMA 移植物的顺应性。e) 在80–120
mmHg 压力范围内,天然肌性动脉与具有 100/0 PCL/PLCL 纤维增强的 gelMA
移植物的顺应性比较,绿色虚线显示小直径血管移植物的目标顺应性值。 f) 在 80–120 mmHg 压力范围内,天然弹性动脉与具有 75/25
PCL/PLCL 纤维增强的 gelMA 移植物的顺应性比较。
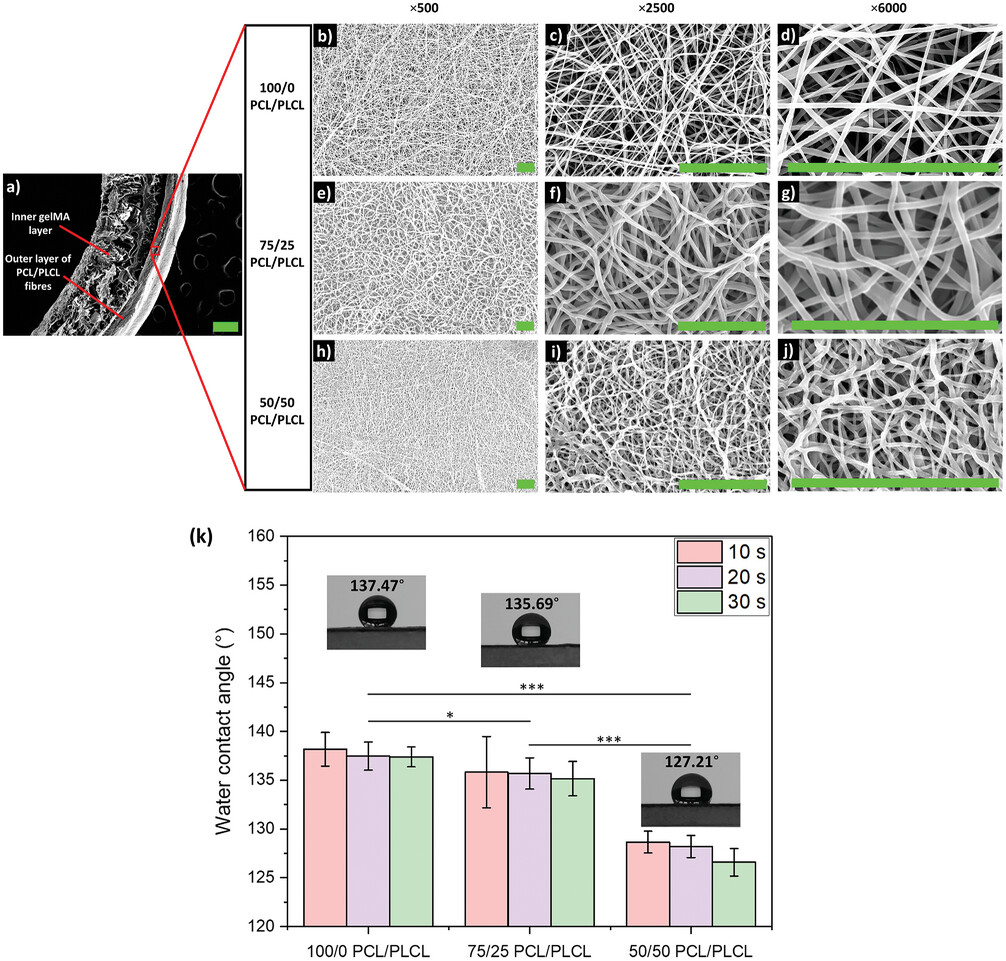
△图5 纤维增强 gelMA 接枝物的微观结构和电纺纳米纤维的润湿性。a) 双层纤维增强
gelMA 结构的 SEM 图像(比例尺:250 µm)。100/0 PCL/PLCL 电纺纳米纤维的 SEM 图像,放大倍数为 b)
×500、c) ×2500、d) ×6000。75/25PCL/PLCL 电纺纳米纤维的 SEM 图像,放大倍数为e) ×500、f)
×2500、g) ×6000。50/50 PCL/PLCL 电纺纳米纤维的 SEM 图像,放大倍数为 h) ×500、i)
×2500、j)×6000(比例尺:20 µm)。 k)水接触角条形图(***,p < 0.001;*,p <
0.05),其中包含每种情况下的典型水滴图像。
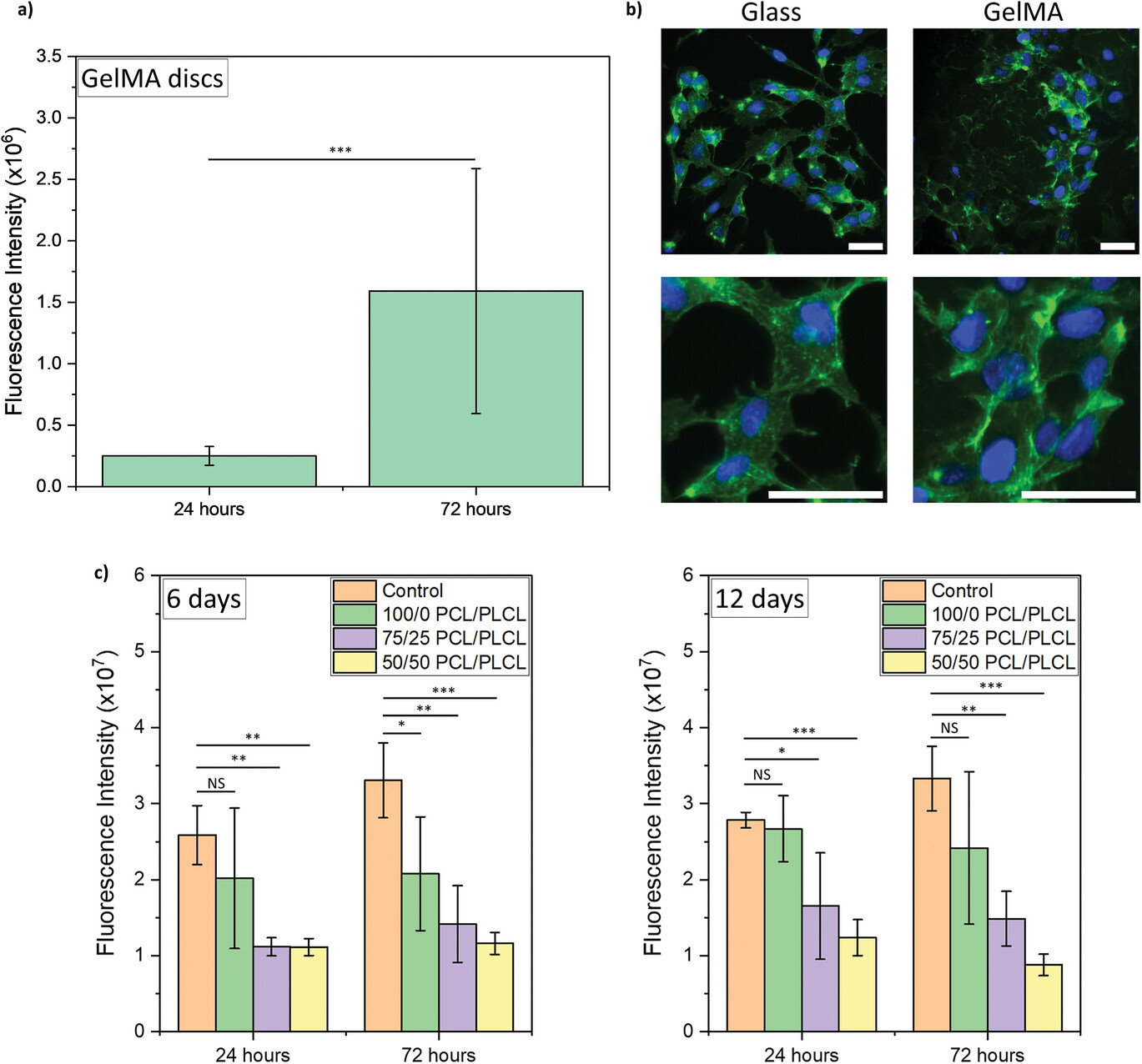
△图6 gelMA 和 PCL/PLCL 电纺纤维的细胞相容性分析。a) 评估 72
小时内 gelMA 圆盘上的 HUVEC 活力。*** p ≤ 0.001。b) 在玻璃和 gelMA 上培养的 HUVEC
的代表性免疫荧光图像,染色为 VE-cadherin(绿色)和 DAPI(蓝色),(比例尺:50 µm)。c) 暴露于电纺纤维浸泡培养基的
HUVEC 活力;支架在培养基中孵育 6 天和 12 天。* p ≤ 0.05,** p ≤ 0.01,*** p ≤ 0.001,NS
不显著。
3D 移植物的厚度范围为直径 1 至 40 毫米,可满足各种应用需求。它们的灵活性意味着它们可以轻松融入人体。研究的下一阶段将涉及研究这些血管在动物身上的使用情况,与爱丁堡大学的罗斯林研究所合作,随后进行人体试验。爱丁堡大学工程学院的主要作者 Faraz Fazal 博士说:“我们的混合技术为组织工程中管状结构的制造开辟了新的和令人兴奋的可能性。”爱丁堡大学工程学院首席研究员 Norbert Radacsi 博士说:“我们的研究成果解决了血管组织工程领域长期存在的挑战——生产出一种具有与人类静脉相似的生物力学特性的导管。有了持续的支持和合作,改善心血管疾病患者治疗方案的愿景可能会成为现实。”
(责任编辑:admin) |